Fosforescencja to luminescencja, która występuje, gdy energia jest dostarczany przez promieniowanie elektromagnetyczne, zwykle światło ultrafioletowe. Źródło energii kopie elektron atom od stanu niższej energii do stanu „wzbudzonego” wyższego stanu energii; następnie elektron uwalnia energię w postaci widzialne światło (luminescencja), kiedy wraca do niższego stanu energetycznego.
Kluczowe informacje: Fosforescencja
- Fosforescencja jest rodzajem fotoluminescencji.
- W fosforescencji światło jest absorbowane przez materiał, co powoduje wzrost poziomów energii elektronów w stan wzbudzony. Jednak energia światła nie do końca pasuje do energii dozwolonych stanów podniecenia, więc pochłonięte zdjęcia utkną w stanie trojaczki. Przejście do niższego i bardziej stabilnego stanu energetycznego wymaga czasu, ale kiedy się pojawi, światło jest uwalniane. Ponieważ to uwalnianie zachodzi powoli, materiał fosforyzujący wydaje się świecić w ciemności.
- Przykłady materiałów fosforyzujących obejmują świecące w ciemności gwiazdy, niektóre znaki bezpieczeństwa i świecącą farbę. W przeciwieństwie do produktów fosforyzujących, pigmenty fluorescencyjne przestają świecić po usunięciu źródła światła.
- Choć nazwano go od zielonej poświaty fosforu pierwiastkowego, fosfor faktycznie świeci z powodu utleniania. To nie jest fosforyzujące!
Proste objaśnienie
Z czasem fosforescencja uwalnia zgromadzoną energię. Zasadniczo materiał fosforyzujący jest „ładowany” przez wystawienie go na działanie światła. Następnie energia jest magazynowana przez pewien czas i powoli uwalniana. Gdy energia jest uwalniana natychmiast po pochłonięciu energii padającej, proces ten jest wywoływany fluorescencja.
Wyjaśnienie mechaniki kwantowej
W przypadku fluorescencji powierzchnia absorbuje i ponownie emituje foton niemal natychmiast (około 10 nanosekund). Fotoluminescencja jest szybka, ponieważ energia zaabsorbowanych fotonów odpowiada stanom energetycznym i dopuszcza przejścia materiału. Fosforescencja trwa znacznie dłużej (milisekundy do dni), ponieważ zaabsorbowany elektron przechodzi w stan wzbudzony z większą krotnością spinu. Podekscytowane elektrony zostają uwięzione w stanie tripletowym i mogą jedynie użyć „zabronionych” przejść, aby spaść do stanu singletowego o niższej energii. Mechanika kwantowa pozwala na zabronione przejścia, ale nie są one kinetycznie korzystne, więc zajmie to więcej czasu. Jeśli wystarczająca ilość światła zostanie pochłonięta, zgromadzone i uwolnione światło staje się na tyle znaczące, że materiał wydaje się „świecić w środku” ciemne. ”Z tego powodu materiały fluorescencyjne, takie jak materiały fluorescencyjne, wydają się bardzo jasne w świetle czarnym (ultrafioletowym). Diagram Jabłońskiego jest powszechnie używany do pokazania różnicy między fluorescencją a fosforescencją.
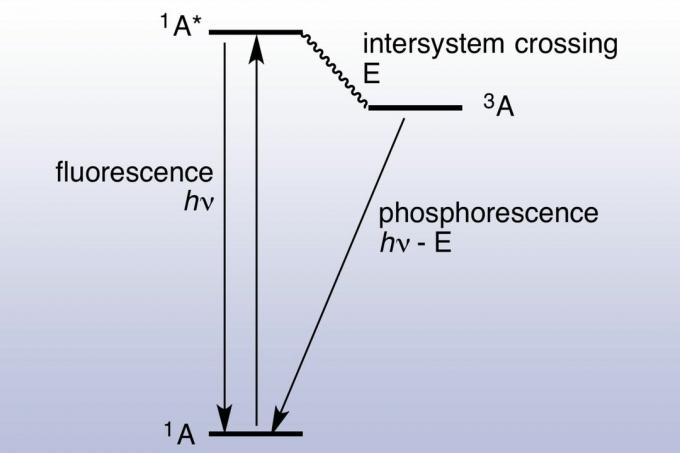
Historia
Badania materiałów fosforyzujących sięgają co najmniej 1602 roku, kiedy włoski Vincenzo Casciarolo opisał „lapis solaris” (kamień słoneczny) lub „lapis lunaris” (kamień księżycowy). Odkrycie zostało opisane w książce profesora Giulio Cesare la Galla z 1612 roku De Phenomenis in Orbe Lunae. La Galla donosi, że kamień Casciarolo emitował na nim światło po tym, jak został zwapniony przez ogrzewanie. Otrzymało światło od Słońca, a następnie (podobnie jak Księżyc) wydało światło w ciemności. Kamień był nieczystym barytem, chociaż inne minerały również wykazują fosforescencję. Obejmują niektóre diamenty (znany królowi indyjskiemu Bhoji już w 1010–1055, ponownie odkryty przez Albertusa Magnusa i ponownie odkryty przez Roberta Boyle'a) i biały topaz. W szczególności Chińczycy docenili rodzaj fluorytu zwanego chlorofanem, który wykazywałby luminescencję od ciepła ciała, ekspozycji na światło lub wcierania. Zainteresowanie naturą fosforescencji i innymi rodzajami luminescencji ostatecznie doprowadziło do odkrycia radioaktywności w 1896 r.
Materiały
Oprócz kilku naturalnych minerałów fosforescencja jest wytwarzana przez związki chemiczne. Prawdopodobnie najbardziej znanym z nich jest siarczek cynku, który jest stosowany w produktach od lat 30. XX wieku. Siarczek cynku zwykle emituje zieloną fosforescencję, chociaż można dodawać luminofory, aby zmienić kolor światła. Fosfory absorbują światło emitowane przez fosforescencję, a następnie uwalniają go w innym kolorze.
Ostatnio glinian strontu stosuje się do fosforescencji. Ten związek świeci dziesięć razy jaśniej niż siarczek cynku, a także magazynuje swoją energię znacznie dłużej.
Przykłady fosforescencji
Typowe przykłady fosforescencji obejmują gwiazdy, które ludzie nakładają na ściany sypialni, które świecą przez wiele godzin po zgaszeniu światła i farby używane do robienia świecących malowideł ściennych. Chociaż element fosfor świeci na zielono, światło jest uwalniane z utleniania (chemiluminescencji) i jest nie przykład fosforescencji.
Źródła
- Franz, Karl A.; Kehr, Wolfgang G.; Siggel, Alfred; Wieczoreck, Jürgen; Adam, Waldemar (2002). „Materiały luminescencyjne” w Encyklopedia chemii przemysłowej Ullmanna. Wiley-VCH. Weinheim. doi: 10.1002 / 14356007.a15_519
- Roda, Aldo (2010). Chemiluminescencja i bioluminescencja: przeszłość, teraźniejszość i przyszłość. Royal Society of Chemistry.
- Zitoun, D.; Bernaud, L.; Manteghetti, A. (2009). Synteza mikrofalowa długotrwałego fosforu. JOT. Chem. Educ. 86. 72-75. doi: 10.1021 / ed086p72