Roztwory buforowe są cieczami na bazie wody, które zawierają zarówno słaby kwas, jak i jego sprzężoną zasadę. Ze względu na swoją chemię roztwory buforowe mogą utrzymywać pH (kwasowość) na prawie stałym poziomie, nawet gdy zachodzą zmiany chemiczne. Systemy buforowe występują w naturze, ale są również niezwykle przydatne w chemii.
Zastosowania rozwiązań buforowych
W układach organicznych naturalne roztwory buforowe utrzymują pH na stałym poziomie, umożliwiając reakcje biochemiczne bez szkody dla organizmu. Kiedy biolodzy badają procesy biologiczne, muszą utrzymywać to samo spójne pH; w tym celu zastosowali przygotowane roztwory buforowe. Roztwory buforowe zostały po raz pierwszy opisane w 1966 r.; wiele takich samych buforów jest dziś używanych.
Aby były użyteczne, bufory biologiczne muszą spełniać kilka kryteriów. W szczególności powinny być rozpuszczalne w wodzie, ale nierozpuszczalne w rozpuszczalnikach organicznych. Nie powinny być w stanie przejść przez błony komórkowe. Ponadto muszą być nietoksyczne, obojętne i stabilne podczas wszystkich eksperymentów, w których są stosowane.
Roztwory buforowe występują naturalnie w osoczu krwi, dlatego krew utrzymuje stałe pH między 7,35 a 7,45. Roztwory buforowe są również stosowane w:
- procesy fermentacyjne
- farbowanie tkanin
- Analiza chemiczna
- kalibracja mierników pH
- Ekstrakcja DNA
Co to jest Tris Buffer Solution?
Tris jest skrótem od tris (hydroksymetylo) aminometanu, związku chemicznego, który jest często stosowany w soli fizjologicznej, ponieważ jest izotoniczny i nietoksyczny. Ponieważ ma Tris, ma pKa 8,1 i poziom pH między 7 a 9, roztwory buforowe Tris są również powszechnie stosowane w szeregu analiz chemicznych i procedur, w tym w ekstrakcji DNA. Ważne jest, aby wiedzieć, że pH roztworu buforowego Tris zmienia się wraz z temperaturą roztworu.
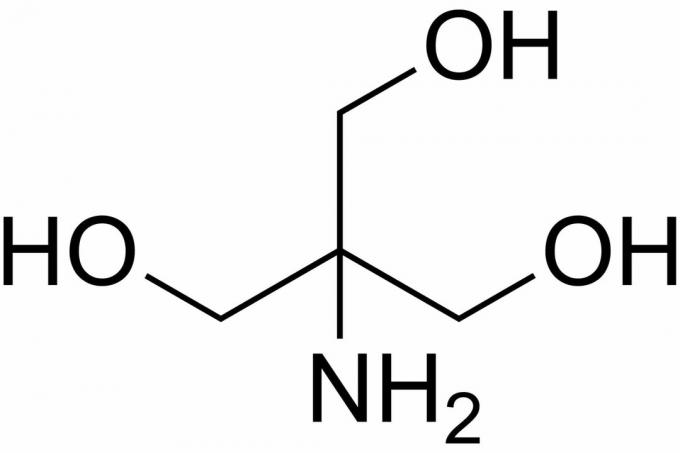
Jak przygotować bufor Tris
Łatwo jest znaleźć dostępne w handlu rozwiązanie buforowe Tris, ale można to zrobić samodzielnie za pomocą odpowiedniego sprzętu.
Materiały:
Oblicz ilość każdego potrzebnego elementu na podstawie stężenia molowego żądanego roztworu i ilości potrzebnego bufora.
- tris (hydroksymetylo) aminometan
- destylowana woda dejonizowana
- HCl
Procedura:
- Zacznij od ustalenia, jakie stężenie (molarność) i objętość bufora Tris, którą chcesz utworzyć. Na przykład roztwór buforowy Tris stosowany w soli fizjologicznej wynosi od 10 do 100 mM. Po podjęciu decyzji o tym, co robisz, oblicz liczbę wymaganych moli Tris, mnożąc stężenie molowe buforu przez objętość tworzonego buforu. (moli Tris = mol / L x L)
- Następnie określ, ile to jest gramów Tris, mnożąc liczbę moli przez masę cząsteczkową Tris (121,14 g / mol). gramów Tris = (moli) x (121,14 g / mol)
- Rozpuść Tris w destylowanej wodzie dejonizowanej, od 1/3 do 1/2 pożądanej objętości końcowej.
- Wmieszaj HCl (np. 1 M HCl) aż do miernik pH daje pożądane pH dla roztworu buforowego Tris.
- Rozcieńczyć bufor wodą, aby osiągnąć pożądaną końcową objętość roztworu.
Po przygotowaniu roztwór można przechowywać przez wiele miesięcy w sterylnym miejscu w temperaturze pokojowej. Długi okres trwałości roztworu buforowego Tris jest możliwy, ponieważ roztwór nie zawiera żadnych białek.